重编程人的内皮细胞至造血干细胞需要血管的诱导
发布时间:2021-12-08 [返回]
研究背景
改造个体的、可移植的造血干细胞和前体细胞具有非常广泛的应用前景。利用体外培养人的多功能干细胞能够分化产生造血前体细胞,但是不能够有效扩增且不能移植到清髓的病人体内。作者实验室之前的研究发现,通过细胞融合可以使体细胞转化为胚胎造血干细胞和前体细胞。但是这个方法的弊端在于不能够长期扩增这类细胞,而且细胞不能多谱系移植。
在本篇研究中,作者发现一套转录因子的组合能够使人的脐带内皮细胞和成人真皮微血管内皮细胞转化为具有多功能干性的造血细胞。内皮细胞的诱导需要无血清血管细胞小室的辅助。
实验结果
名词注解:
FGRS:转录因子组合:FOSB,GFI1,RUNX1,SPI1
HUVECs:人脐带内皮细胞
hDMECs:成人真皮微血管内皮细胞
rEC-hMPP:内皮细胞转化的具有多功能干性的造血细胞
hES-ECs:人胚胎干细胞诱导的内皮细胞
HSC:造血干细胞
HSPCs:造血干细胞和前体细胞
细胞类型:
HSPCs: Lin-CD34+
HUVECs: CD45-CD133-c-Kit-CD31+
HSCs:hCD45+Lin-hCD45RA-hCD38-hCD90+hCD34+
MMPs: hCD45+Lin-hCD45RA-hCD38-hCD90-hCD34+
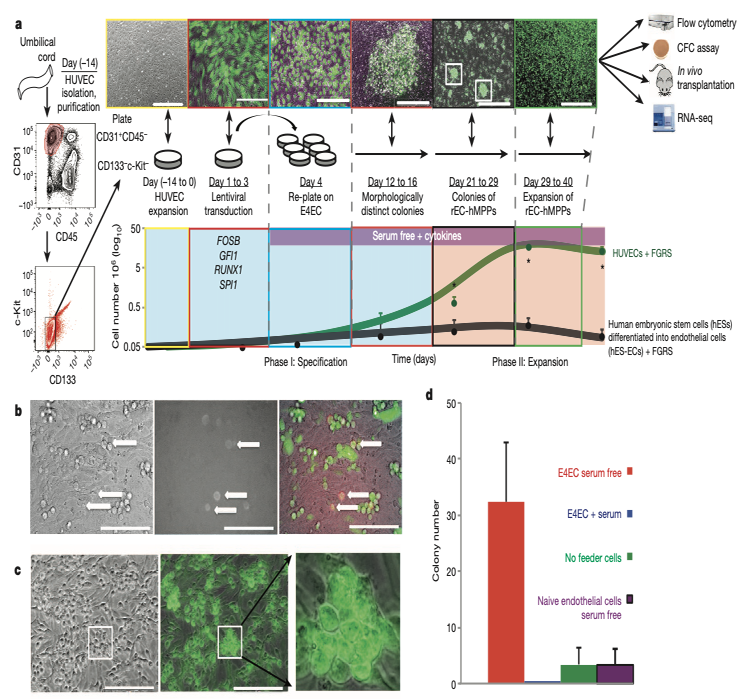
一、通过FGRS转录因子和血管细胞诱导HUVECs和hES-ECs转化为造血细胞
造血干细胞是从血管床中产生的。因此,作者推测血管小室对维持和诱导造血干细胞具有不可或缺的功能。作者通过在内皮细胞中过表达腺病毒的E4ORF1基因(E4ECs)构建了血管小室的模型。E4ECs细胞能够在无血清的情况下生长。
在构建好基底细胞E4ECs细胞充当血管小室之后,作者通过以下步骤将HUVEC细胞诱导为rEC-MPP细胞。首先将分离的HUVEC细胞体外培养扩增,并使用慢转录病毒将FGRS转录因子转HUVEC细胞中,其中GFP阳性的细胞表示成功表达了FGRS基因;其次,将慢病毒感染后的HUVEC细胞铺到E4EC细胞中培养;最后,HUVEC细胞能够形成细胞群落,并能够进一步扩增(图1a)。HUVEC细胞和E4EC细胞共培养2周左右,诱导产生CD45+GFP+的葡萄状细胞群落(图1b)。在3-4四周之后,形成类似于造血细胞一样的细胞群落(图1c)。但是血清的存在会显著抑制细胞群落的形成以及CD45阳性细胞的产生(图1d)。
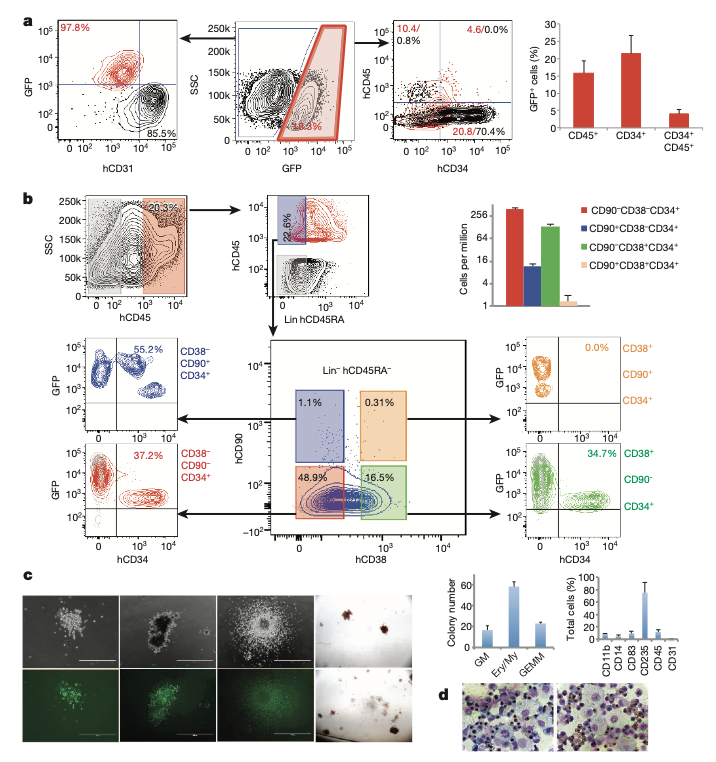
二、rEC-hMMPs在功能上和表型上重现多干性 HSPCs
为了进一步厘清由HUVECs细胞诱导产生的细胞特征,作者进行了详细的分析。诱导产生的细胞中有18%的细胞是GFP阳性的细胞,然而GFP阳性的细胞基本都是失去了内皮细胞的标志心分子CD31,并开始出现表达造血细胞的分子CD45(图2a)。当分析GFP阳性细胞时,发现这群细胞出现CD45阳性具有免疫表型的干细胞和多功能前体细胞(图2b)。
虽然表型上HUVECs细胞能够被诱导产生HSPC细胞,但是其具有HSPC的功能有待验证。因此,作者将GFP+hCD45+hCD34+分选处理进行集落形成细胞分析。由HUVECs细胞分化产生的HSPC细胞能够有效的产生粒细胞/巨噬细胞;红细胞;树突状细胞和巨核细胞(图2c和d)。因此,rEC-hMPP细胞是具有功能的多谱系前体细胞。
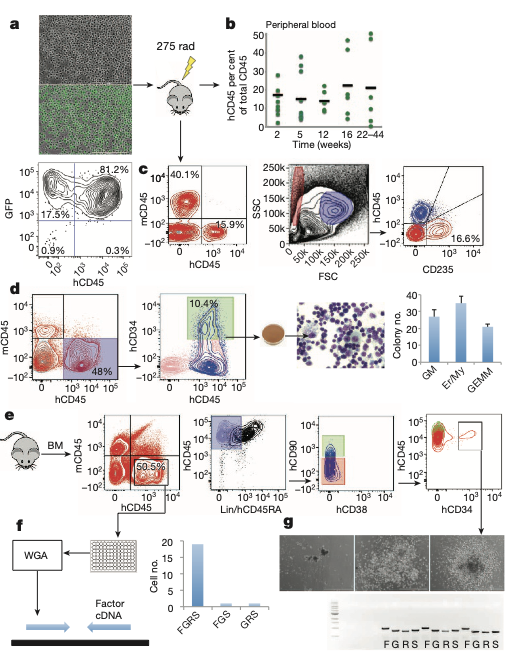
三、rEC-hMPPs具有体内红细胞-髓细胞-巨核细胞多谱系移植能力
在验证rEC-hMPP细胞具有多谱系干性之后,作者进一步验证其体内移植潜力。将HUVEC诱导产生的rEC-MPP细胞移植到致死剂量辐照的免疫缺陷的小鼠体内(图3a),并在不同时间检测受体小鼠外周血中hCD45分子表达情况。作者发现到44周时,hCD45分子的表达情况与第2周相差无几(图3b)。在通过分析发现,受体小鼠体内能够产生hCD45-hCD235+的红细胞(图3c)。这两点说明,rEC-hMPP能够成功移植到受体小鼠且分化产生红细胞。作者将hCD45+hCD34+细胞分选处理进行体外的集落形成细胞分析,发现这群细胞能够分化产生粒细胞/巨噬细胞;红细胞;树突状细胞和巨核细胞(图3d)。此外,为了验证FGRS基因集合对HUVECs诱导产生rEC-hMPP是否是必须的。作者将rEC-hMPP进行单细胞分析,并分析FGRS基因整合情况(图3e-g)。从小鼠体内分选出来的细胞中,21个细胞中19个细胞同时包含FGRS四个基因(图3f)。当把小鼠体内的hCD45+细胞分选出来进行集落形成细胞分析,发现所有细胞群里都包含FGRS四个基因(图3g)。
四、功能性和转录分析hDMEC诱导的rEC-hMPPs
作者将该技术进一步推广到成年人内皮细胞中,检验其适用性。作者将成年人的真皮微血管内皮细胞分离进行体外培养,并通过慢病毒导入FGRS基因集合随后与E4ECs细胞进行诱导培养,然后将GFP+hCD45+hCD34+细胞分选出来进行功能分析和小鼠移植实验(图4a)。作者发现这类细胞能够具有造血细胞的形态而且能够分化产生不同的髓系细胞(图4b)。通过转录组分析对比rES-hMPP细胞在移植到小鼠体内前后,发现rES-hMPP在移植22周后,hCD45+hCD34+的rES-hMPP细胞从转录组上跟接近骨髓造血干细胞和前体细胞,相对的下调了血管细胞的转录本(图4c)。当与胚胎干细胞的转录本进行对比时,发现多能干性基因并没有在rES-hMPP中被明显上调(图4d)。
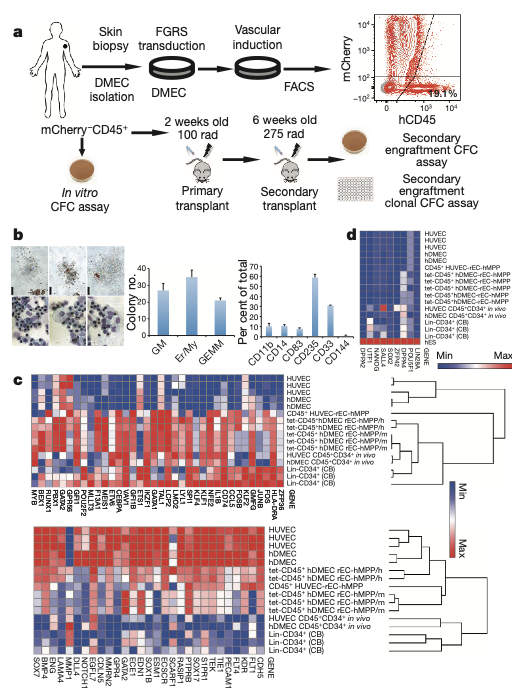
五、成人hDMEC诱导的rEC-hMPPs在体内具有原代和二次移植能力
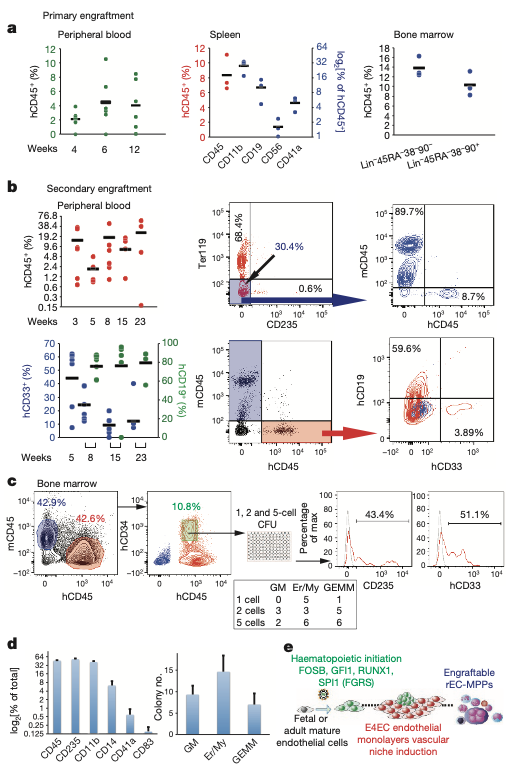
将r-EC-hMPP细胞移植到致死剂量辐照的免疫缺陷小鼠体内,在第4周开始检测到外周血中循环的hCD45+细胞,并且在14周后的脾脏细胞中能够检测到髓系细胞和淋巴细胞(图5a)。此外,在小鼠骨髓中还能检测到HSC细胞和MPP细胞(图5a)。
因为HSC细胞和MPP细胞具有自我更新的能力,所以作者借此验证rEC-hMPP在小鼠体内产生的HSC和MPP细胞是否也同样具有这方面的能力。因此,作者将接受移植的小鼠体内的rEC-hMPP细胞分选出来进行二次移植,并在不同时间检测外周血发现接受二次移植的小鼠体内产生hCD45+细胞(图5b),其中包括髓系细胞和淋巴细胞。因此,rEC-hMPP细胞具有自我更新的能力。
再者,作者论证单个的rEC-hMPP细胞是否具有多谱系潜力。作者分别分选1个,2个和5个hCD34+hCD45+细胞到96孔板中进行集落形成细胞分析,发现单个细胞也能分化产生髓系细胞,巨核细胞和红细胞(图5c和d)。
总结与讨论
对于治疗造血系统的疾病,改造可移植的自体细胞具有非常广阔的医疗前景。本文中作者创造了体外改造内皮细胞使其诱导产生多功能干性细胞。这类细胞具有以下特征:
1.体外扩增能力
2.多功能干性
3.可移植特性
4.自我更新能力
5.无成癌风险
手机:400-878-2661 邮箱:service@antihela.com 联系人:王先生
技术支持:厦门易尔通网络科技有限公司 闽ICP备15018136号-1 公安备案:












